 |
 |
|
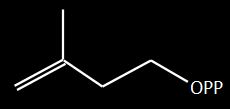
A rota de biossíntese dos isoprenóides é há muito tempo conhecida, săo muitos os produtos naturais, metabólitos secundários, que seguem a rota sintética dos terpenóides. Os terpenóides săo classificados quanto ao número de átomos de carbono, săo eles: os hemiterpenos (C5), monoterpenos (C10), sesquiterpenos (C15), diterpenos (C20), triterpenos (C30) e tetraterpenos (C40). Dentro dessas classes de substâncias podemos destacar as piretrinas, os óleos essenciais compostos por inúmeras substâncias, como mentol e linalol, o fitol presente na clorofila e os carotenoides. |
 |
|
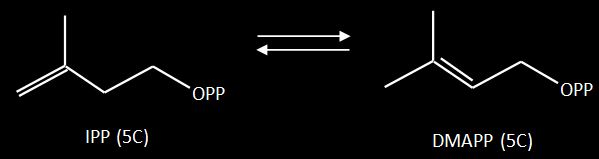
Os carotenoides săo tetraterpenos com 40 átomos de carbono sintetizados por bactérias, algas, fungos e plantas superiores. Com exceçăo de alguns poucos carotenoides produzidos por bactérias, que apresentam 30, 45 ou 50 átomos de carbono. Foram descobertas duas rotas para a formaçăo do Isopentenilpirofosfato (IPP - Figura acima) que é a unidade primária da síntese dos terpenóides. Uma característica de plantas e bactérias e outra de fungos. Os carotenoides de fungos săo derivados da via do mevalonato, na qual o ácido mevalônico é sintetizado via condensaçăo de tręs moléculas de acetil-SCoa. Os passos subseqüentes envolvem etapas de fosforilaçăo, gerando ácido mevalônico pirofosfato, que sofre descarboxilaçăo para gerar IPP. Em bactérias e nos plastídios de plantas a formaçăo do IPP se dá via rota alternativa conhecida como 1-desoxyxilulose-5-fosfato, que é o primeiro intermediário da rota, ou de 2-C-metil-D-eritritol-4-fosfato que é o primeiro produto. Uma vez que a enzima IPP isomerase está presente nos plastídios de plantas, pode-se concluir que IPP é o produto majoritário ou único da via 1-desoxyxilulose-5-fosfato. O DMAPP deve ser originado através da isomerizaçăo do IPP (Figura abaixo). |
|
O farnesil pirofosfato (FPP), com 15 átomos de carbono, é o produto seguinte na rote de biossíntese. Ele é formado através da açăo de diferentes enzimas prenil transferases, que após a isomerizaçăo do IPP para DMAPP e mediante tręs condensaçőes cabeça-cauda (C1´- C4) com unidades IPP. |
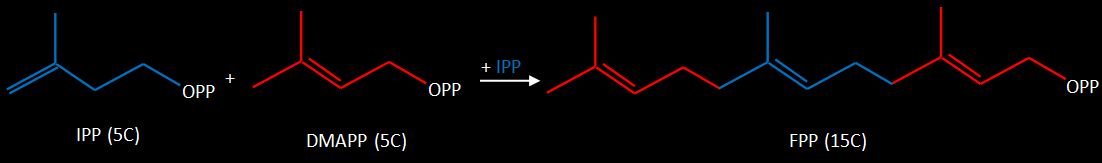 Formaçăo do Farnesil Pirofosfato (FPP) com 15 Carbonos
|
O próximo produto na rota de biossíntese dos carotenoides é o Geranilgeranil pirofosfato, agora com a metade dos átomos de carbono das moléculas características dos carotenoides, 20. Para sua formaçăo, as reaçőes continuam sendo catalisadas pelas enzimas prenil transferases e seguem o mecanismo de acoplamento cabeça-cauda, tanto em plantas superiores quanto em bactérias.
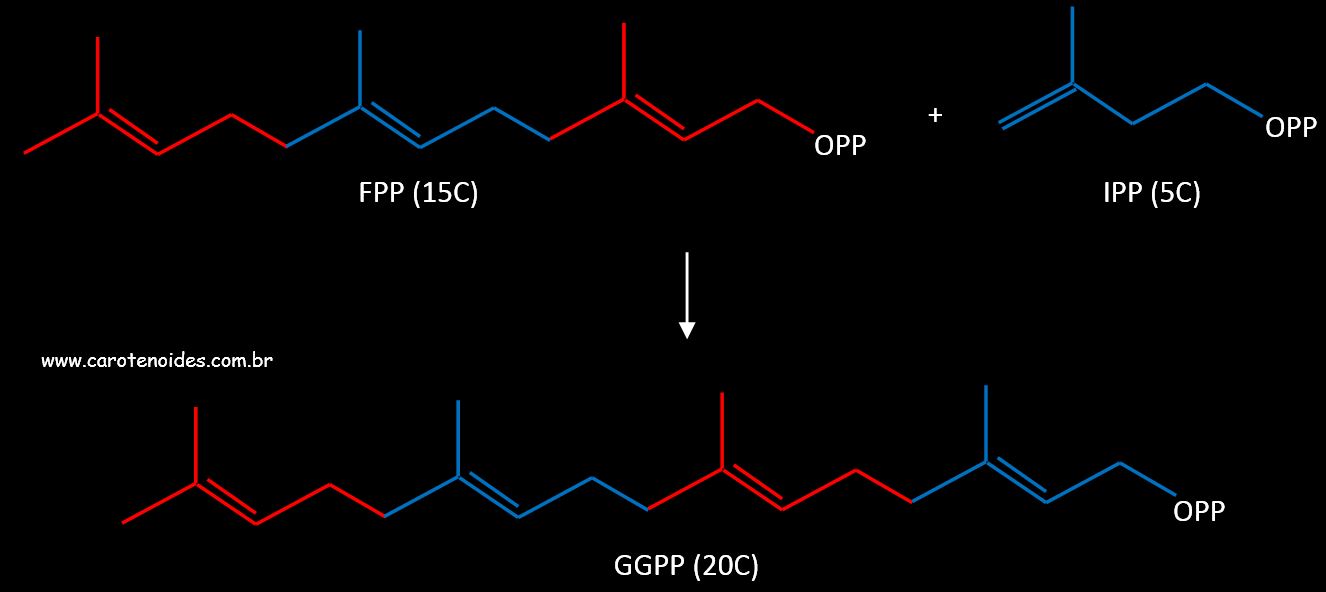 Formaçăo do Geranilgeranil Pirofosfato (GGPP) com 20 Carbonos
A síntese da primeira substância com 40 átomos de carbono, que é reconhecida como o primeiro carotenoide precursor dos demais, é realizada agora através de uma condensaçăo cabeça-cabeça de duas moléculas de GGPP. A reaçăo forma um intermediário ciclopropilcarbonil entre os carbonos C1 da primeira unidade GGPP e os carbonos C2 e C3 da segunda molécula de GGPP. Com a eliminaçăo do grupo pirofosfato (desfosforilaçăo), e com a abstraçăo estereoespecífica de um hidrogęnio (H+), chega-se ao fitoeno. Este apresenta 9 ligaçőes duplas, sendo apenas 3 conjugadas (no centro da molécula). 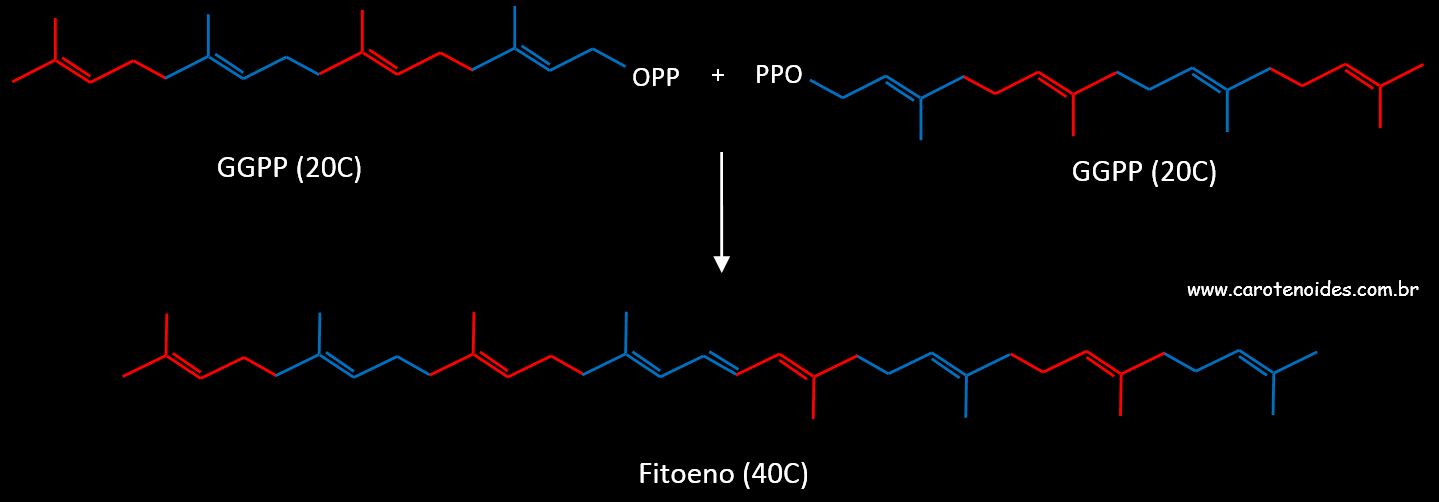 Formaçăo do Carotenoide Fitoeno, a partir de duas moléculas de Geranilgeranil Pirofosfato (GGPP)
Após a formaçăo do Fitoeno, as reaçőes que se seguem tem por finalidade aumentar a insaturaçăo (duplas ligaçőes) das moléculas e, na sequęncia, ciclizar e inserir funçőes oxigenadas, como hidroxilas e carbonilas. Os produtos na sequęncia da rota de biossíntese săo os carotenoide fitoflueno, com 5 duplas ligaçőes conjugadas (5 DLC), e o zeta-caroteno. Produzido através da açăo da enzima fitoeno desidrogenase após quatro etapas de desidrogenaçăo, e consequente formaçăo de mais 2 duplas ligaçőes, o zeta-caroteno apresenta agora 11 ligaçőes duplas, sendo 7 delas conjugadas no centro da molécula (7 DLC). 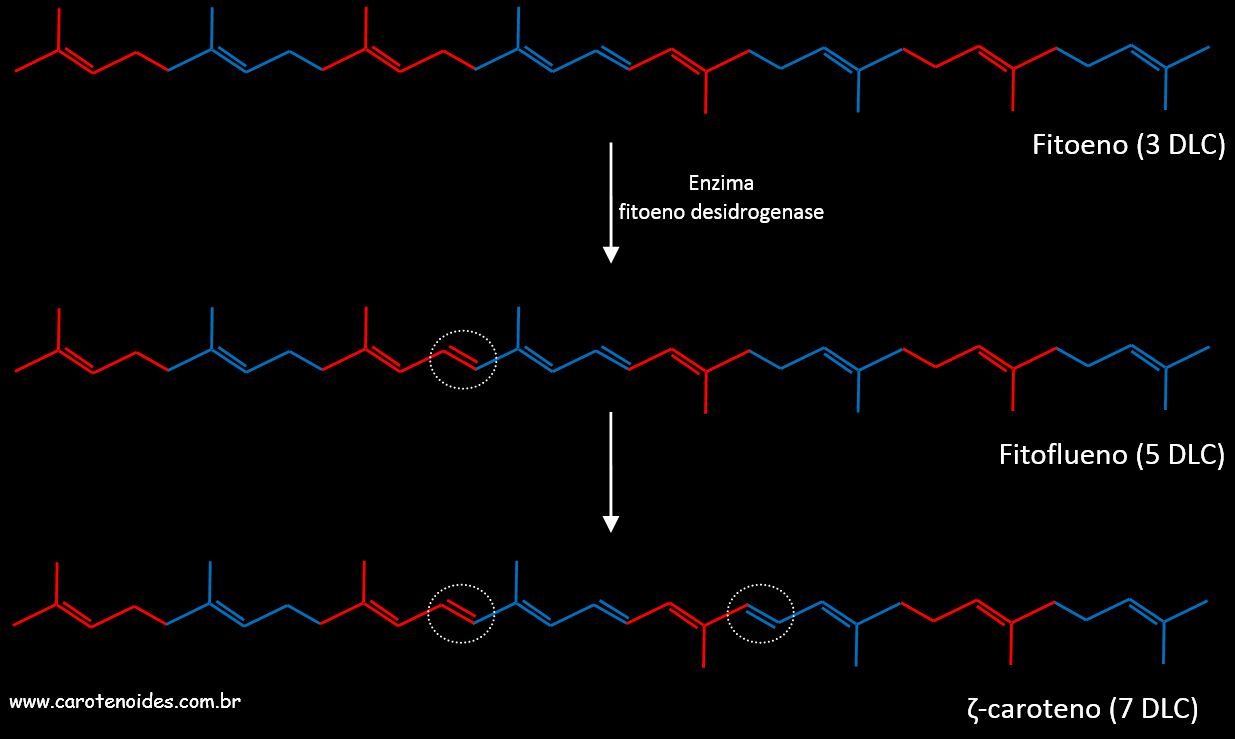 Formaçăo dos carotenoides fitoflueno (5 DLC) e zeta-caroteno (7 DLC) a partir do Fitoeno
A coloraçăo caracteristica dos carotenoides só tem início a partir da sétima ligaçăo conjugada (7 DLC), isto considerando a visăo humana. Desta maneira, os carotenoides fitoeno (3 DLC) e fitoflueno (5 DLC) săo incolores, enquanto o zeta-caroteno (7 DLC) apresenta coloraçăo amarela pálida. Na página Cor e espectros UV/Vis esta questăo é abordada mais a fundo. A desidrogenaçăo do fitoeno prossegue até a obtençăo do Neurosporeno (9 DLC) e do Licopeno, este é o carotenoide de plantas com o maior número de ligaçőes duplas conjugadas (11 DLC). Como consequencia das 11 DLC o Licopeno apresenta agora coloraçăo vermelha intensa, característica do tomate, melancia e goiaba vermelha. 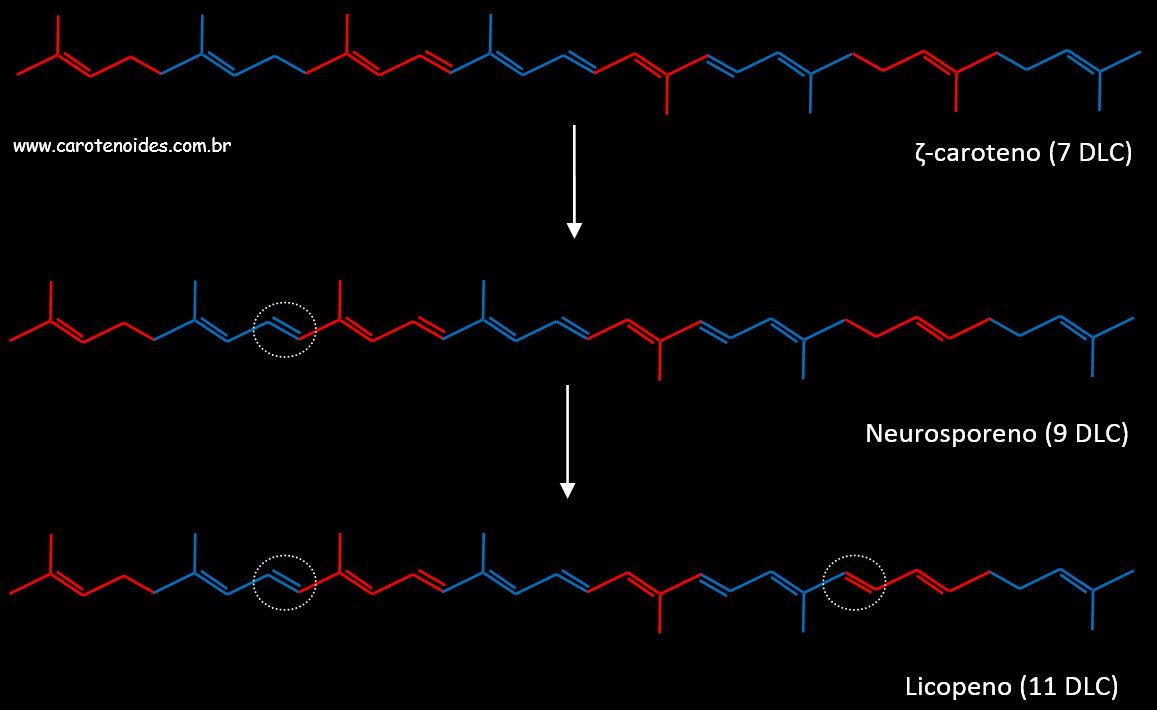 Formaçăo dos carotenoides Neurosporeno (9 DLC) e Licopeno (11 DLC) a partir do zeta-caroteno
O licopeno é o precursor dos carotenóides cíclicos, o mecanismo da ciclizaçăo que forma o anel beta envolve a adiçăo estereoespecífica de um hidrogęnio no carbono C2. Tem-se por pressuposto que a reaçăo de ciclizaçăo dos carotenóides é similar, em princípio, ao processo de ciclizaçăo na biossíntese de outros compostos isoprenóides. A enzima ciclase envolve o final da cadeia alquílica colocando-a em conformaçăo adequada (Figura abaixo).
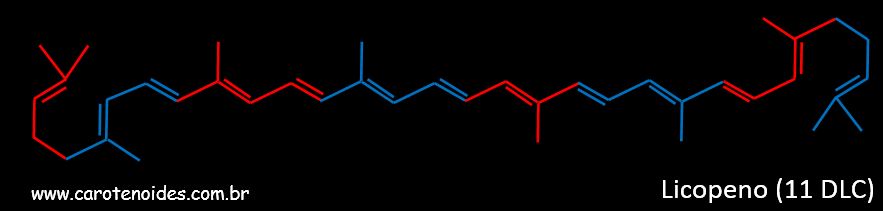 O carotenoide Licopeno (11 DLC) com as extremidades em conformaçăo adequada para a ciclizaçăo
Após esta conformaçăo, ocorre um ataque eletrofílico em C2, com conseqüente formaçăo da ligaçăo C1-C6 para formaçăo do anel. Esse mecanismo leva ŕ formaçăo de um carbocátiom em C5 estabilizado pela enzima. Com a eliminaçăo de hidrogęnio ocorre a formaçăo do anel. Se a saída do H+ for de C6 tem-se a formaçăo do anel beta-ionona, se for de C4 o anel epson, e se a saída for do grupo metil, tem-se a formaçăo do anel gama.
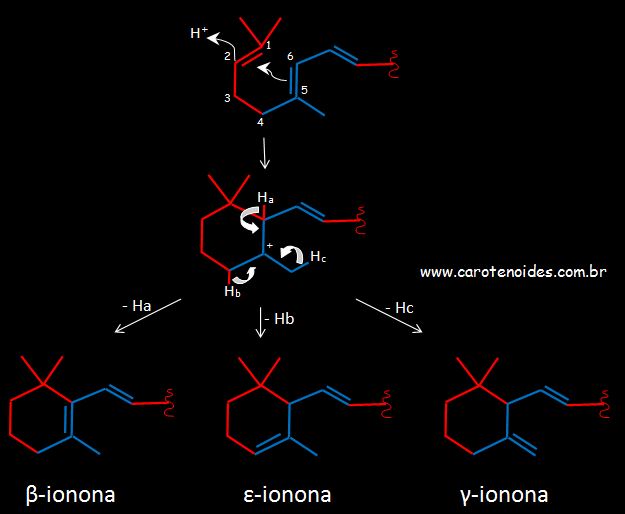 Ciclizaçăo das extremidades do Licopeno formando os anés beta, epson e gama ionona
A ciclizaçăo do Licopeno pode ocorrer apenas em uma ou nas duas extremidades, combinando ainda os tręs anéis ionona possíveis. Desta maneira, o número de substâncias que podem ser geradas é grande. Dentre as substâncias destacam-se o beta-caroteno e o alfa-caroteno, mais exemplos de substâncias podem ser encontrados na página Estruturas Químicas.
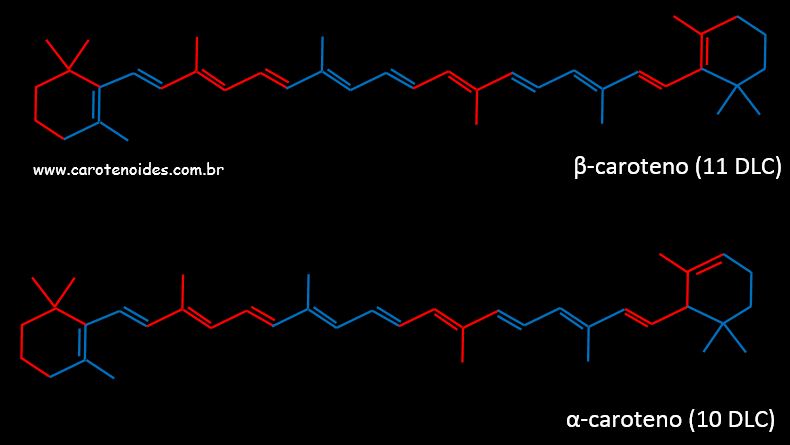 Exemplos de derivados cíclicos do Licopeno, os carotenoides alfa e beta-caroteno
As xantofilas, que săo os carotenóides oxigenados, săo enzimaticamente formadas pela oxidaçăo do alfa-caroteno e beta-caroteno. Grupos típicos săo hidroxilas na posiçăo C3 dos anéis beta e eposn-ionona, epóxido nas posiçőes C5,6 do anel beta-ionona e o grupo cetona na posiçăo C4. Inúmeros exemplos destas substâncias podem ser encontrados na página Estruturas Químicas.
|